Covid-19 - overvågning
| Ugentlig vurdering covid-19 |
|---|
|
Smitteniveau Spildevand Indlæggelser Virusvarianter |
Året rundt overvåger vi covid-19 for at kunne opdage eventuelle stigninger i smittetilfælde og nye varianter af virussen og deres alvorlighed. Derudover overvåger vi tilslutningen til vaccinationsprogrammet for covid-19.
Omfanget af personer med covid-19-sygdom i befolkningen bliver yderligere overvåget ved systematisk indsamling af ugentlige data og prøver blandt andet fra de praktiserende læger i sentinelovervågningen, som er geografisk fordelt over hele landet og vagtlægeordningen. Antallet af patienter med covid-19, indlagt på hospital, bliver fulgt ved hjælp af data fra landspatientregisteret.
Den seneste uges covid-19-overvågningsdata bliver offentliggjort her på siden hver onsdag eftermiddag. Samtidig bliver der offentliggjort yderligere detaljerede ugedata på vores interaktivecovid-19-dashboards.
Laboratoriebekræftet covid-19
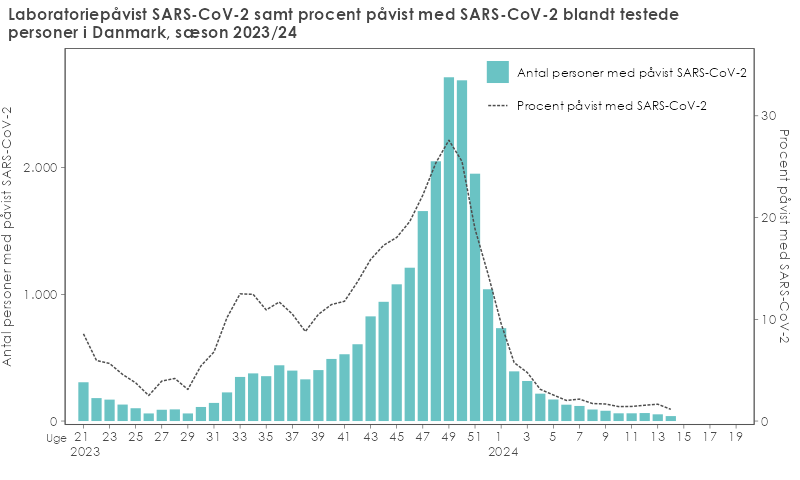
Det totale antal laboratoriepåviste smittetilfælde af SARS-CoV-2 i Danmark bliver opgjort ugentligt ved udtræk fra den danske mikrobiologidatabase (MiBa). På den måde kan vi overvåge antallet af patienter, der er positive for covid-19 per uge, og hvor stor en andel af de testede patienter som er positive for covid-19.
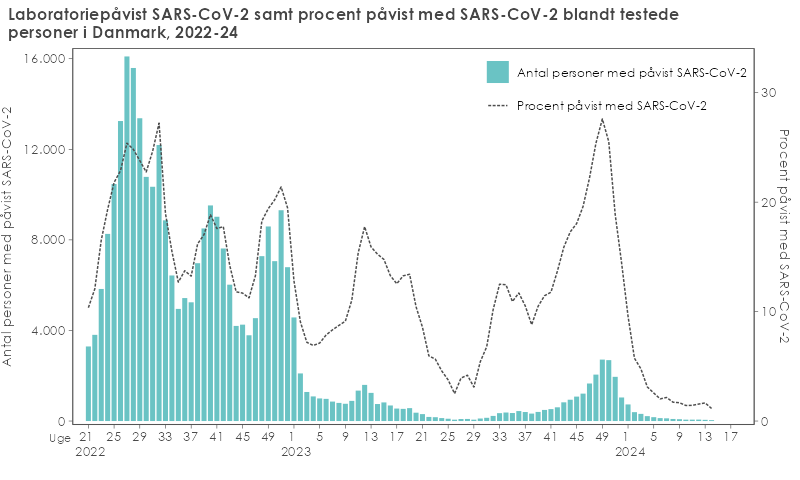
Graferne herunder viser antallet af påviste smittetilfælde, og andelen af personer der tester positiv blandt alle testede personer. Data bliver vist samlet for alle aldersgrupper for uge 21 og frem i indeværende sæson (2023/24) samt for uge 21 og frem i 2022.
Variantovervågning
Vi følger udvalgte SARS-CoV-2-virusvarianter, som formodes at give et alvorligere sygdomsforløb og/eller være mere smitsomme, og/eller har nedsat følsomhed for antistoffer. De 8 hyppigst observerede (sub)varianter ud fra helgenomsekventeringsdata følges på ugentlig basis og sammenholdes med de øvrige virologiske overvågningsdata med henblik på at give en kvalificeret vurdering af status på varianter den seneste uge.
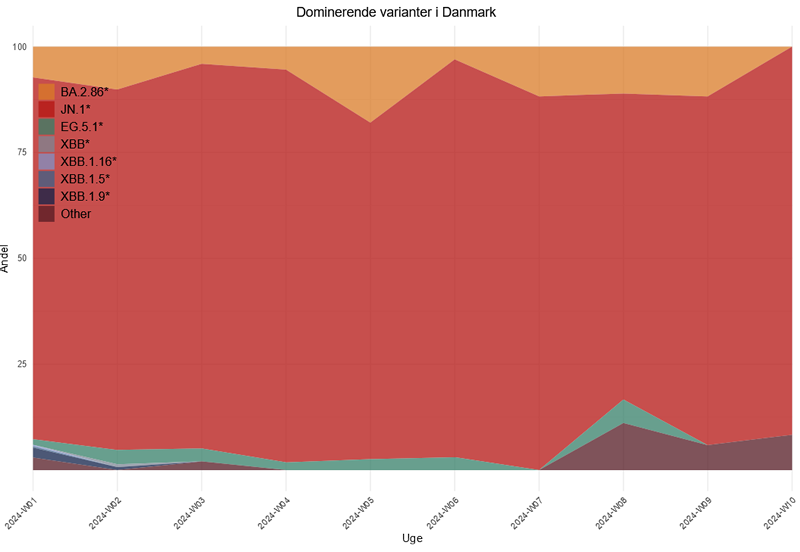
Her kan du læse mere om de forskellige virusvarianter: covid-19-virusvarianter.
Spildevandsovervågning
Spildevandsresultaterne giver mulighed for at følge smitteudviklingen nationalt og regionalt og vurdere om forekomsten af SARS-CoV-2 er i vækst eller ej. Spildevandsovervågningen dækker ca. 47% af befolkningen og prøverne bliver udtaget to gange ugentligt fra 29 prøvetagningssteder fordelt over hele landet. Her bliver udvalgte områder i landet overvåget ugentligt, hvor man måler mængden og vækstrater af covid-19 virus i spildevandet. Den nationale vækstrate, der viser den gennemsnitlige ugentlige vækst over de seneste tre uger, bliver vurderet på ugentlig basis. Du kan finde flere detaljer om spildevandsovervågningen her.
Grafen herunder viser forekomsten af SARS-CoV-2 i spildevand samlet for alle prøveudtagningssteder og antal nyindlæggelser på grund af SARS-CoV-2 virus i Danmark. Grafen bliver opdateret ugentligt.
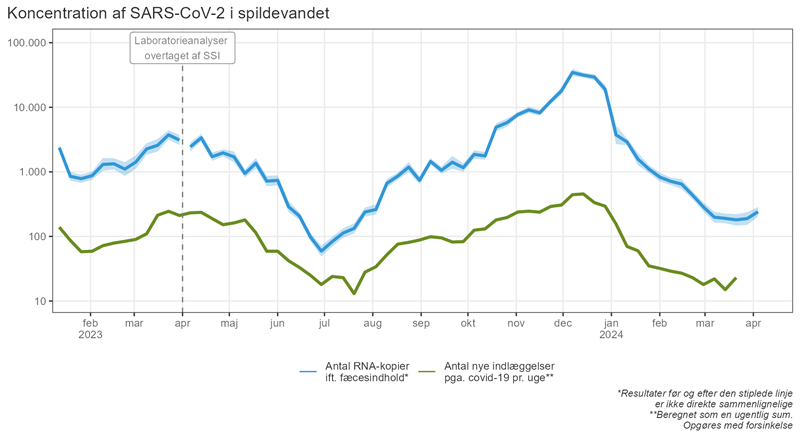
Her kan du læse mere om spildevandsovervågning: national overvågning af SARS-CoV-2 i spildevandet.
Vaccinationstilslutning
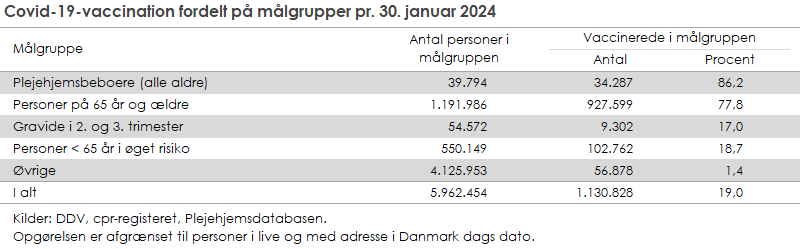
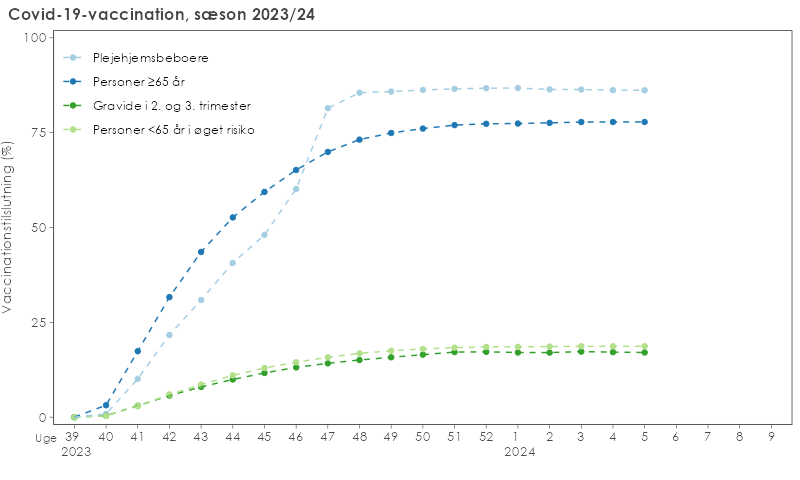
Fra 1. oktober 2023 til 15. januar 2024 bliver udvalgte målgrupper tilbudt vaccination mod covid-19. Tabellen viser fordelingen af personer i de forskellige covid-19-målgrupper og andelen af vaccinerede indenfor hver målgruppe ved afslutningen af vaccinationssæsonen. Tallene vil derfor ikke længere blive opdateret her på siden.
Interaktive dashboards om covid-19
Her finder du en fælles indgang til alle vores dashboards: interaktive dashboards
Historisk arkiv med covid-19-opgørelser
I perioden 12. marts 2020 til 25. oktober 2023 overvågede vi løbende forekomsten af covid-19 ved hjælp af en række epidemiologiske og virologiske data samt gennemførte detaljerede opgørelser, analyser og målinger. Derudover udgav vi ugentlige tendensrapporter for covid-19 og andre luftvejsinfektioner i perioden 28. oktober 2021 til 30. marts 2023.
Du kan finde en del af dette materiale i vores historiske arkiv: Historiske covid-19-opgørelser.